环肽在肽偶联药物研发中的新进展
发布时间:
2024-06-26
作者:
戴秋云 博士,中晟全肽研发战略部副总级顾问
1、环肽的基本特性与优势
环肽包括天然及合成环肽,合成环肽是线性肽(类肽)通过环化反应形成的环形分子,有单环、双环及多环形式。相比线性肽,环肽具有活性高、结构限制性大、抗酶解及透膜性能力强等特点,双环肽或多环肽的对靶点选择性更高,可与抗体相比拟[1]。目前已有不少天然环肽及合成环肽药物上市,在FDA或EMA批准的60多个多肽药物中,环肽占2/3[2]。近年来,多肽通过连接子偶联其他分子,如抗癌药物(毒素)、放射螯合物、小核酸、小分子等,拓宽了多肽药物分子形式及使用范围,使非靶向药物成为靶向药物,大大降低药物的毒性并提高药效。环肽在肽偶联毒素药物(peptide-drug conjugates, PDC)及肽偶联核素药物(Radionuclide-drug conjugates, RDC,也属PDC)尤为重要,环肽PDC较线性肽PDC稳定,比抗体偶联药物(antibody-drug conjugates)更易渗透到固体瘤组织,制备相对容易、成本低等。环肽RDC具有在体内停留少、副作用低、可兼顾治疗及诊断等优势(图1)。
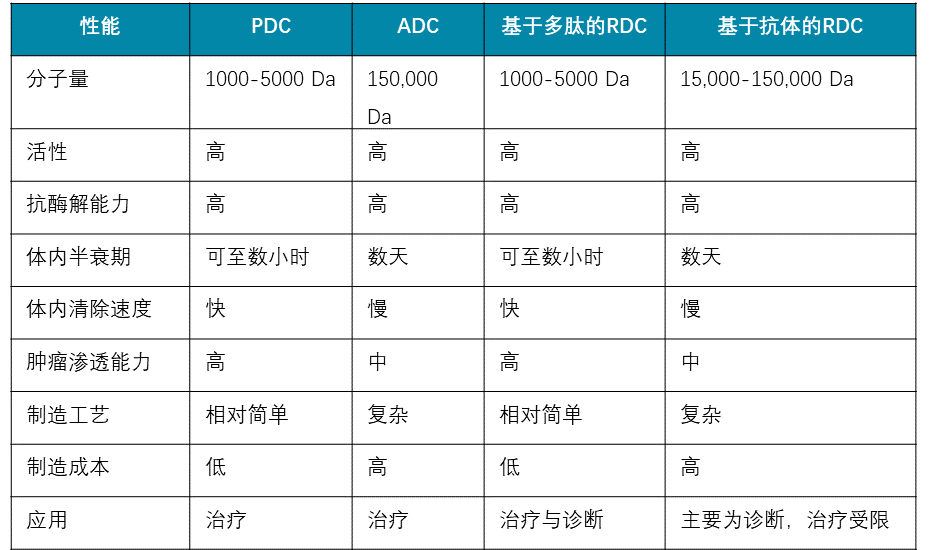
图1. 基于环肽的PDC、RDC与抗体偶联药物的性能比较
2、环肽偶联药物PDC、RDC的研发进展
2.1 环肽的PDC
当前环肽PDC发展较快,涉及靶标较多,如Nectin-4、EPHA2、MT1-MMP、金属蛋白酶14(MMP14)、SSTR2、ɑvβ3、ɑvβ6、Her2、GRPR、FAP、CXCR4、EDB-FN等[3,4]。一些进入临床试验的典型环肽PDC见图2。在双环肽PDC方面,Bicycle Therapeuticals公司进展迅速,目前已有多个双环肽药物进入临床I-III期(图2、3)。
2024年ASCO会议,Bicylce Therapeutics公布了其BT8009(靶向Nectin-4)和BT5528(靶向EphA2)安全性数据。最新的临床试验结果显示,BT8009(受试149例)的3级及以上TRAEs发生率为31%(截至2024年3月22日), BT5528(受试74例)的3级及以上TRAEs发生率为22%(截至2024年3月14日)(图4)。在BAT8009和BT5528给药患者中,周围神经病变、皮肤反应、中性粒细胞减少症、眼部疾病、高血糖等3级及以上TRAEs发生率均较低。Bicylce Therapeutics认为BT8009的安全性比同一靶点的上市ADC Enfortumab Vedotin高,Enfortumab Vedotin在确认性III期研究中,EV组的3级及以上TRAEs发生率为51.4%。上述BT8009及BT5528的最新临床安全性数据表明,只要靶向肽及Payload合适, PDC并不一定比ADC副作用高。若BT8009临床III期试验依然显示好的安全性及有效性,将会大大加强医药界对PDC的关注及发展。
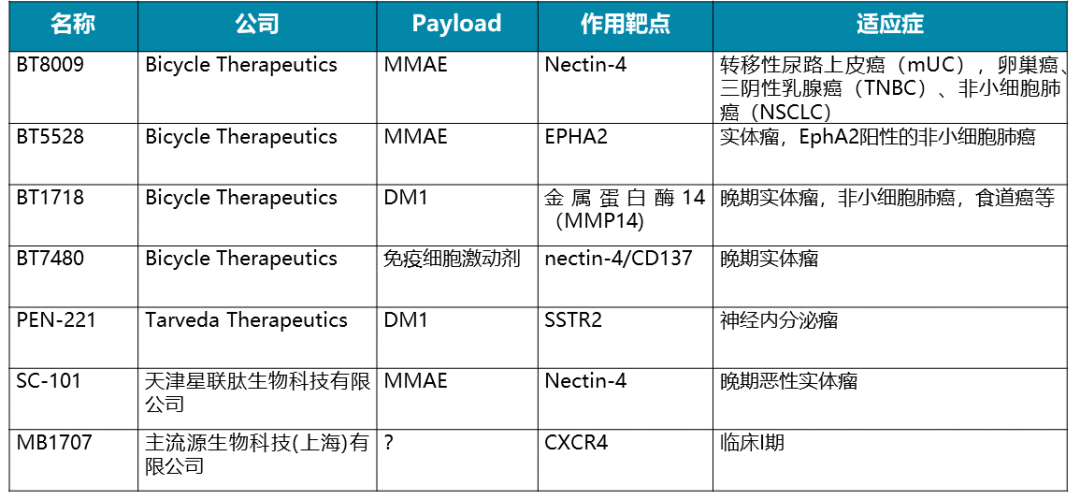
图2. 处于临床研究阶段的典型环肽PDC
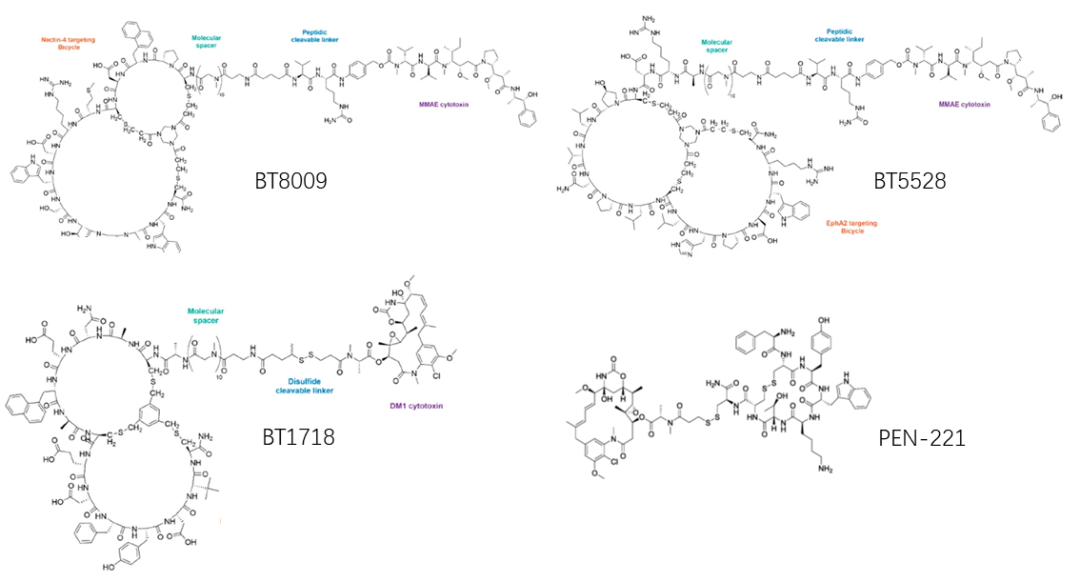
图3. 部分处于临床试验的环肽PDC典型的结构式[6,7]
注:靶向分子为单环、双环或三环,多为双环分子;数据来自各公司网站
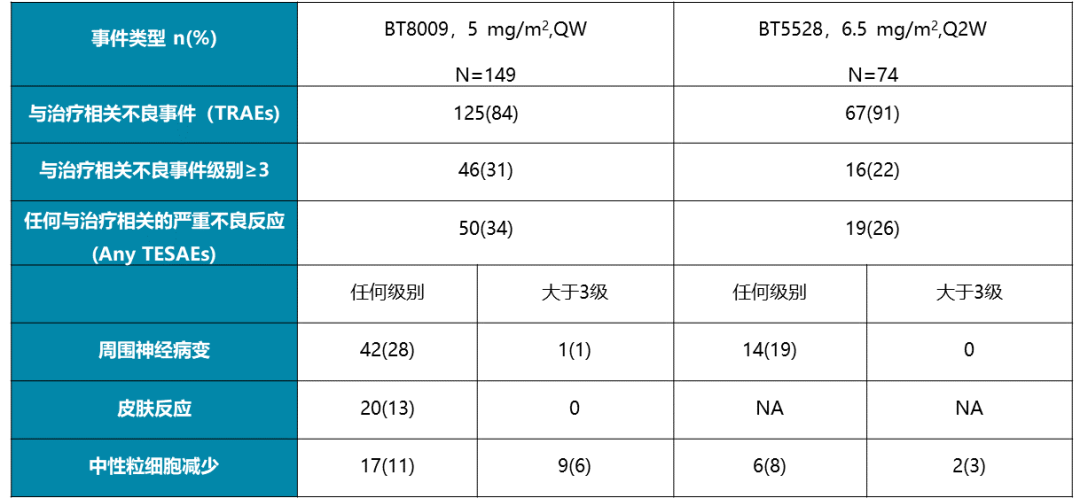
图4. PDC BT8009及BT5528的I-II期安全性数据[5]
2.2 环肽的RDC
目前为止,已批准上市9个RDC,其中4个为环肽RDC(图5),用于胃肠胰腺神经内分泌肿瘤治疗与诊断。由于RDC发展较晚,大部分环肽RDC处于临床前或活性测定阶段[8],进入临床研究的环肽RDC靶点主要集中在SSTR、MC1R、αvβ3、αvβ6等(图5)[9,10],涉及的放射性同位素主要有177Lu、68Ga、64Cu、90Y、18F、225Ac及212Pb等,177Lu、90Y、225Ac及212Pb用于治疗,68Ga、64Cu及18F用于PET诊断。因225Ac的α射线的杀伤距离比较长,可以弥补177Lu杀伤距离短的缺点,而212Pb发射α射线及β射线,通过多步衰变最终形成稳定的同位素208Pb,环境友好。最近这两种核素在RDC设计中受到关注,但目前225Ac供应受限,工业化的212Pb生产还不成熟。总之,目前RDC是非常有效的癌症治疗方法,环肽在RDC中将占主要地位,随着新靶点的开发以及临床前试验的成熟,将会有更多的环肽RDC进入临床试验或批准上市。
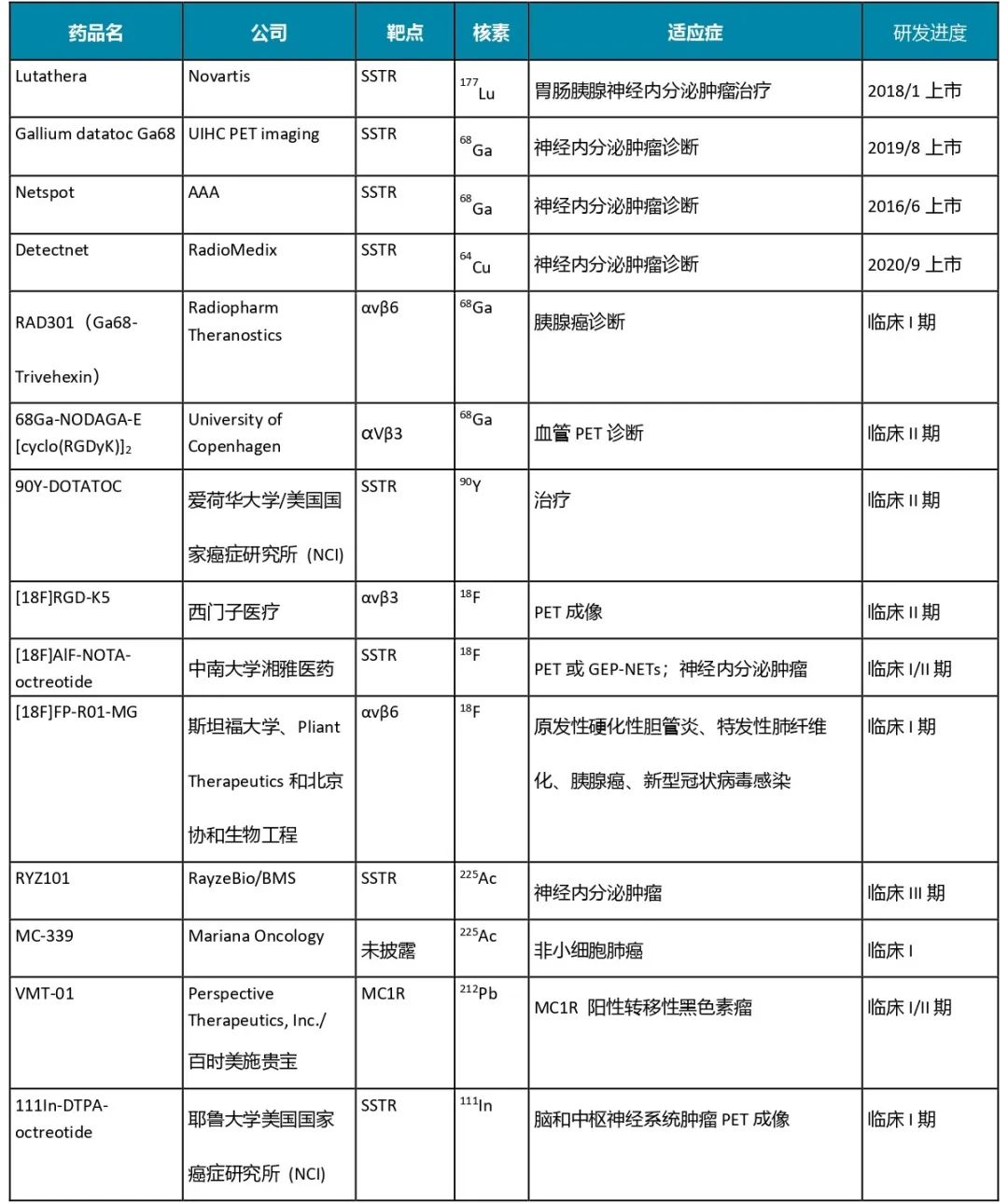
图5. 已上市及处于临床研究的环肽RDC[9,10]
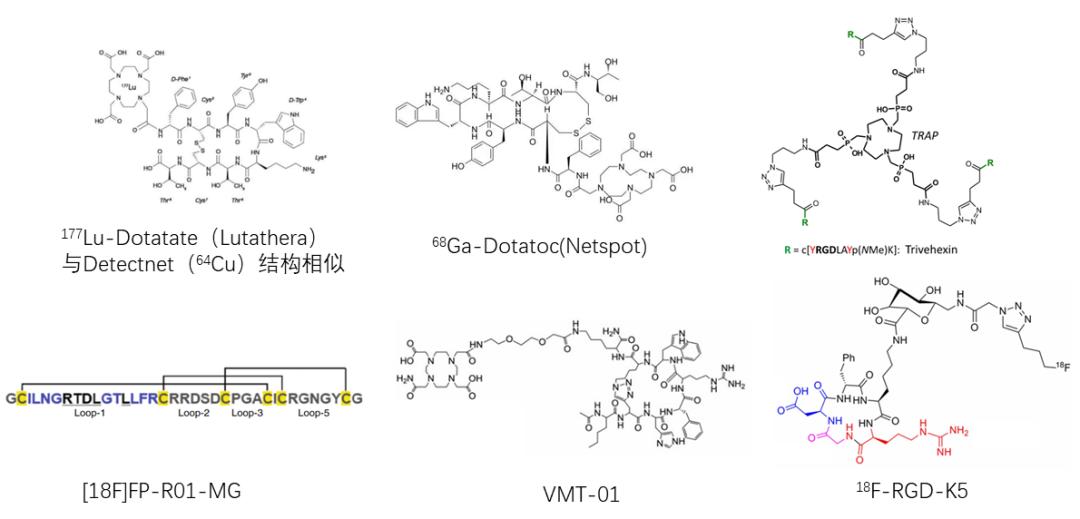
图6. 部分上市及处于临床实验环肽RDC药物的结构式[9,11]
注:靶向分子为单环多肽,如奥曲肽、cyclo(RGDfK)、突变的MSH环肽等;放射金属离子螯合配体大部分为DOTA、NOTA;数据来自各个公司网站
3、环肽的合成技术
在环肽PDC及RDC的研发中,环肽靶分子一般是通过筛选或分子改造而来,为筛选及活性验证需要合成含天然氨基酸或其他氨基酸、小分子基团的环肽。
3.1 单环肽合成方法
(1) 不含二硫键环肽的合成方法
单环肽合成可以采用首尾环化、侧链与N-端或C-端偶联、侧链与侧链偶联等策略[11,12],如侧链胺基或羧基,可与C-端的羧基或N-端的氨基偶联。如多肽中除偶联的活性基团外,无其他活性基团,可以脱保护后进行偶联,否则带保护基在溶液相或固相上进行,然后裂解除去保护基,得到粗肽。在采用氨基与羧基缩合策略成环中,时常采用特殊保护的氨基酸,在完成多肽链组装后再脱保缩合,如氢化、肼、氟化物等可脱除的交叉保护氨基酸。除通过酰胺键成环策略外,还可以通过氨基与醛基还原胺化[13]、巯基与一些亲电试剂反应[14,15]、羟基与羧基反应关环、偶联反应等实现成环[16]。
(2) 含二硫键环肽的合成方法
对于疏水性不大的含一对二硫键的多肽,可先脱除保护剂,线性肽在中性或偏碱性条件下,空气氧化形成二硫键,也可采用DMSO、Fe3+、碘等氧化[17]。对于疏水性很高的多肽,采用水溶液体系或含一定溶剂的体系氧化收率比较低,此时可以在树脂上用碘氧化脱Acm关环,然后裂解纯化[18]。
3.2 双环肽或多环肽合成方法
双环肽及多环肽的环化方法较多,可以通过氨基、羧基、羟基、巯基、烯键、炔键、卤代芳烃等通过氨酸缩合、成酯、偶联、click等各种策略进行成环(图7)[1,19~21]。对于含多对二硫键的环肽,对巯基采用Acm、酸敏感保护基Mmt或光敏感基团等进行分别保护,然后进行分步折叠氧化或脱保护偶联[22]。

图7. 一些双环肽的构建路线[18]
目前已发展一些一步环化合成双环肽的连接体(图8),这些连接体的活性基团与巯基、氨基或叠氮基团反应成环。该类反应迅速,收率较好,已用于开发双环肽药物。此类环化要注意去氧、溶剂选择及pH值,反应在澄清溶液中进行,溶剂有乙腈、DMF等,溶剂比例不应太高,以免影响关环及纯化。
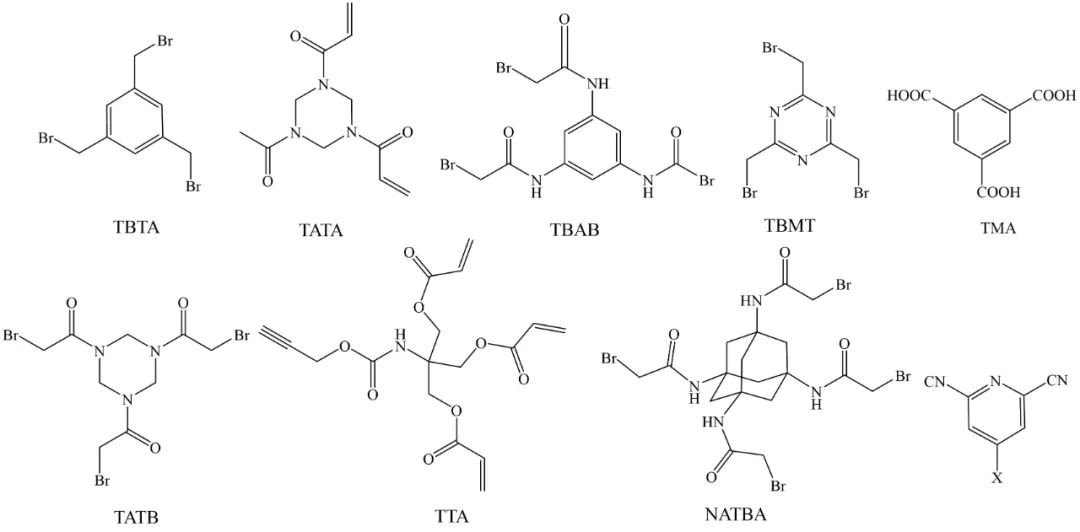
图8.常见的双环肽连接体分子结构
总的来说,环肽PDC及RDC的合成还是有一定难度,如复杂环肽及多环肽合成、环肽+linker与毒素的偶联等,需要熟练掌握多肽合成及小分子合成技巧,方能获得产率高的目标产物。
4、环肽及其偶联药物(PDC或RDC)投资活跃,市场前景广阔
随着降糖及减肥药物司马格鲁肽的应用,多肽药物的重要性受到普遍关注,尤其是司马格鲁肽2023年的销售额超过200亿美金,震惊医药界。目前口服环肽、环肽PDC及RDC等在全球受到重点关注,为下一波创新药的重要类型。早在2017年,诺华以39亿美元收购了Advanced accelerator applications(AAA)公司的环肽放射性偶联药物Lutathera,次年又收购Endocytede 的Pluvicto和255Ac-PSMA-617的权益。2023年Pluvicto及Lutathera 的销售额分别为9.8及6.05亿美元,诺华收获丰厚。当前,一些环肽发现、环肽PDC及RDC公司,如Bicycle Therapeutics、Peptidream等,受到诺华、默克等重点投资或收购,受让公司自身发展迅速,股价飙升或获得巨大回报。图9仅列出了2023.5-2024.6一些重点的环肽及其PDC、RDC相关投融资交易事件,可见环肽PDC及RDC领域投融资十分活跃,前景诱人。
据弗若斯沙利文数据,2020年多肽的全球市场规模为625亿美金,中国多肽药物市场为587亿元。华经产业研究院预计2025年全球多肽药物市场规模达到960亿美元。在大环肽和订书肽的药物市场方面,有一份报告预测[23],2024-2030年,仅将从目前的 12.2亿美元增至47.6亿美元,如加上其他环肽、PDC及RDC,市场规模将远超这个数额。
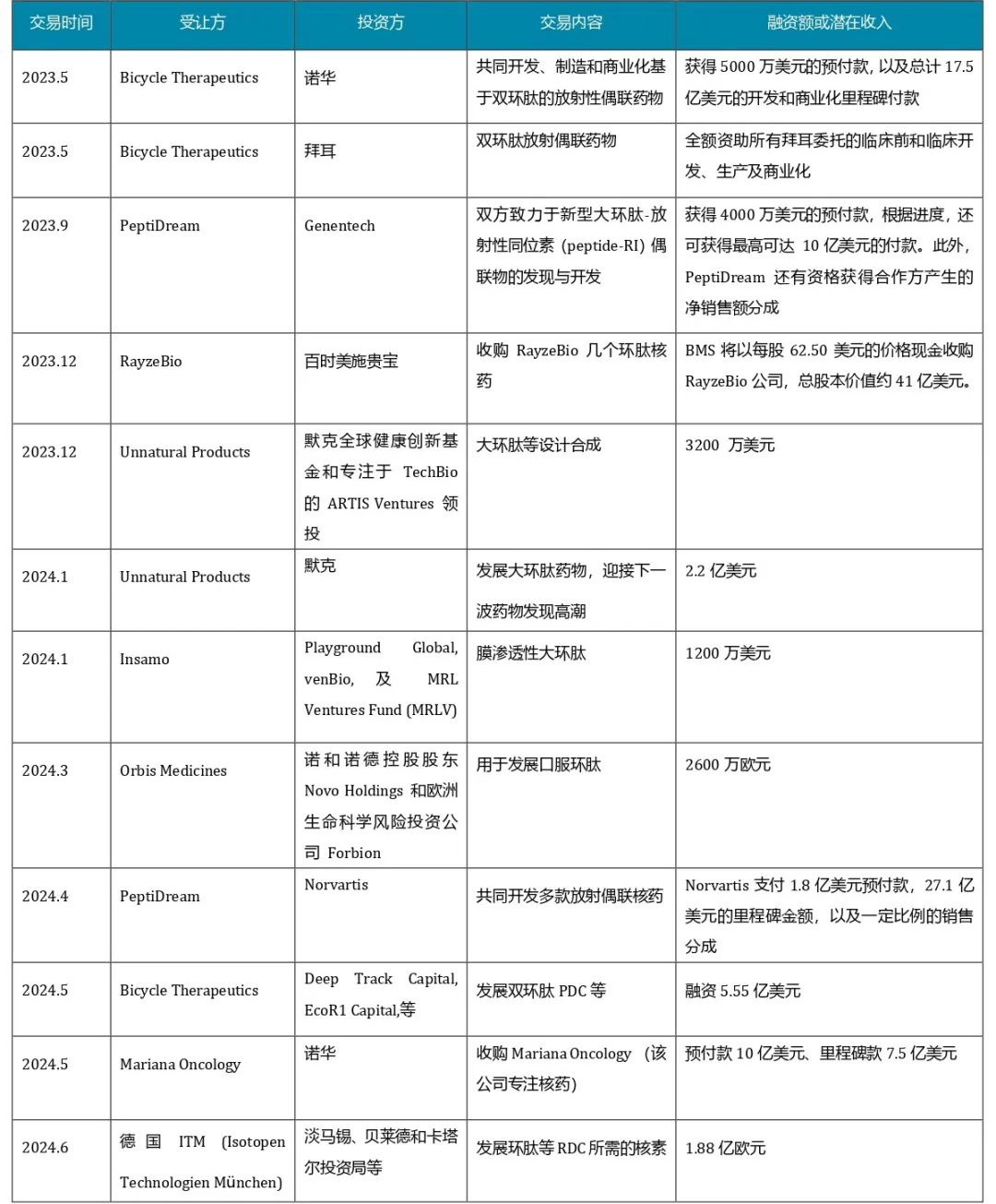
图9. 2023-2024年一些环肽药物融资事件(数据来自各公司网站)
5、中晟全肽已具有复杂环肽及其偶联药物筛选、设计及合成技术,正在为本公司PDC、RDC项目及其他公司服务
湖南中晟全肽生物科技股份有限公司是一家以推动全球多肽新药研发领域创新的生物医药技术企业,致力于成为全球领先的药物发现新引擎。公司成立于2017年9月,总部位于中国株洲,在美国新泽西设有子公司。中晟全肽拥有全球独创的多肽信息压缩技术(PICT),已构建完成包含近五亿种多肽信息的超大型多肽实体库及噬菌体多肽库、动物多肽库、纳米环肽库、虚拟多肽库等四大互补性分子发现库,为多肽新药发现提供了全球独一无二的“种子库”,解决了全球多肽新药发现端“卡脖子”技术难题。公司也拥有成熟的环肽AI分子设计、复杂环肽及其偶联药物的合成技术,正在为公司的PDC、RDC项目及其他公司服务。
参考文献
- 1. Buckton LK, Rahimi MN, McAlpine SR. Cyclic Peptides as Drugs for Intracellular Targets:The next frontier in peptide therapeutic development.Chemistry. 2021,27(5):1487-1513.
- 2. Zhang H, Chen S. Cyclic peptide drugs approved in the last two decades (2001-2021). RSC Chem Biol. 2021,3(1):18-31.
- 3. Fu C, Yu L, Miao Y, et al. Peptide-drug conjugates (PDCs): a novel trend of research and development on targeted therapy, hype or hope? Acta Pharm Sin B. 2023,13(2):498-516.
- 4. Wang M, Liu J, Xia M, et al. Peptide-drug conjugates: A new paradigm for targeted cancer therapy. Eur J Med Chem. 2024,265:116119.
- 5. 2024年ASCO会议报告
- 6. Buyanova M, Cai S, Cooper J, et al. Discovery of a bicyclic peptidyl Pan-Ras inhibitor. J Med Chem. 2021, 64(17):13038-13053.
- 7. Mudd GE, Scott H, Chen L, et al. Discovery of BT8009: A nectin-4 targeting bicycle toxin conjugate for the treatment of cancer. J Med Chem. 2022,65(21):14337-14347.
- 8. Senior M. Precision radiation opens a new window on cancer therapy. Nat Biotechnol. 2024 Jun 12. doi: 10.1038/s41587-024-02295-z. Epub ahead of print.
- 9. Quigley NG, Steiger K, Hoberück S, et al. PET/CT imaging of head-and-neck and pancreatic cancer in humans by targeting the "Cancer Integrin" αvβ6 with Ga-68-Trivehexin. Eur J Nucl Med Mol Imaging. 2022,49(4):1136-1147.
- 10. Orcutt KD, Henry KE, Habjan C, et al. Dosimetry of [212Pb]VMT01, a MC1R targeted alpha therapeutic compound, and effect of free 208Tl on tissue absorbed doses. Molecules. 2022,27(18):5831.
- 11. Hussein WM, Skwarczynski M, Toth I. Peptide synthesis Methods and Protocols, Humana press, 2020.
- 12. Khazaei-Poul Y, Farhadi S, Ghani S, Ahmadizad SA, Ranjbari J. Monocyclic peptides:tTypes, synthesis and applications. Curr Pharm Biotechnol. 2021,22(1):123-135.
- 13. Li B, Wang L, Chen XX, et al. Extendable stapling of unprotected peptides by crosslinking two amines with o-phthalaldehyde. Nat Commun, 2022,13(1):311.
- 14. Merz ML, Habeshian S, Li B, et al. De novo development of small cyclic peptides that are orally bioavailable. Nat Chem Biol. 2024,20(5):624-633.
- 15. Chen H, Zhang Q. Native peptide cyclization, sequential chemoselective amidation in Water. J Am Chem Soc. 2023,145(50):27218-27224. doi: 10.1021/jacs.3c10341.
- 16. Wang P, Liu J, Zhu XM, et al. Synthesis of clickable peptides via late-stage maleimidation on C(7)-H tryptophan. Nat Commun.2023, 14, 3973.
- 17. Wang S, Bartels P, Zhao C, et al. A 4/8 Subtype α-Conotoxin Vt1.27 inhibits N-Type calcium channels with potent anti-allodynic effect. Front Pharmacol. 2022,13:881732.
- 18. Liu J, Xu S, Huang C, Shen J, et al. Synthesis and activity evaluation of selenazole-coupled CPI-1 irreversible bifunctional inhibitors for botulinum toxin A light chain. Bioorg Med Chem Lett. 2022,73:128913.
- 19. Ahangarzadeh S, Kanafi MM, Hosseinzadeh S, Mokhtarzadeh A, Barati M, Ranjbari J, Tayebi L. Bicyclic peptides: types, synthesis and applications. Drug Discov Today. 2019,24(6):1311-1319.
- 20. Ji X, Nielsen AL, Heinis C. Cyclic peptides for drug development. Angew Chem Int Ed Engl. 2024,63(3): e202308251.
- 21. Johns DG, Campeau LC, Banka P, et al. Orally bioavailable macrocyclic peptide that inhibits binding of PCSK9 to the low density lipoprotein receptor. Circulation. 2023,148(2):144-158.
- 22. Qiu Z, Dai X, Fan C, et al. A new regioselective synthesis of the cysteine-rich peptide linaclotide. Molecules. 2023, 28(3):1007.
- 23. "Global constrained peptide drugs market by peptide type (macrocyclic, stapled), end-user (Hospitals & Clinics, Pharmaceutical Companies) - Forecast 2024-2030"
*声明:本文仅是介绍医药疾病领域研究进展或简述研究概况或分享医药相关讯息,并非也不会进行治疗或诊断方案推荐,也不对相关投资构成任何建议。



